Industria7 de agosto, 2019
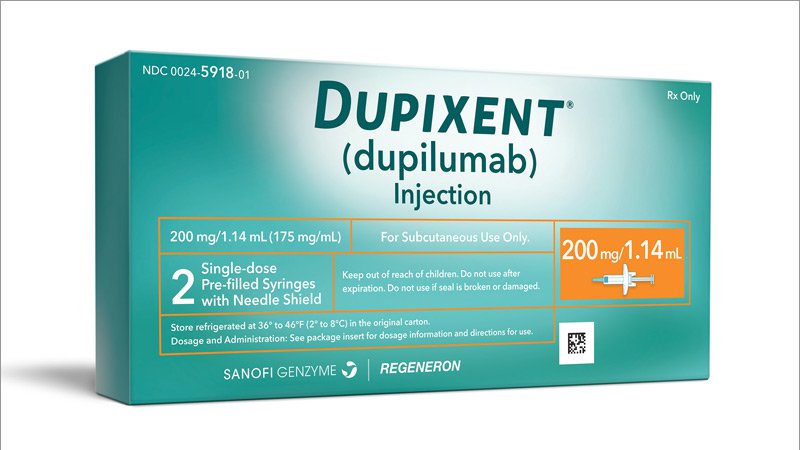
La Comisión Europea aprueba Dupixent® (dupilumab) para adolescentes con dermatitis atópica moderada a grave
Pharma Market
NOTICIAS RELACIONADAS
Jordi Sánchez, Bayer España: "Apostamos por la inversión en España y cómo Hub de innovación global"
La Comisión Europea (EC) ha extendido la autorización de comercialización para Dupixent® (dupilumab) en la Unión Europea (UE) para adolescentes entre 12 y 17 años con dermatitis atópica moderada a grave, que son candidatos a una terapia sistemática. Dupixent es ahora la primera medicina biológica aprobada en la UE para tratar a estos pacientes.
"La dermatitis atópica moderada a grave puede afectar en muchos afectos la vida de los adolescentes, incluyendo su bienestar físico y emocional", sostiene Christine Janus, CEO de la Alianza Internacional de Organizaciones de Pacientes con Dermatología. "Esta enfermedad supone una carga inmensa no sólo para los jóvenes sino también para las personas que viven con ellos y los familiares que los cuidan. Nosotros agradecemos la incorporación de nuevas opciones de tratamiento para ayudar a los adolescentes a controlar una enfermedad a menudo agotadora".
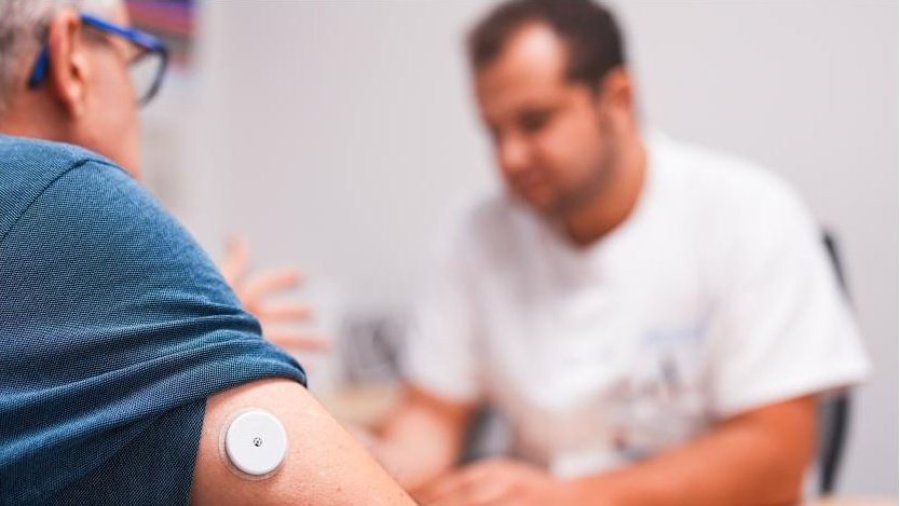
La dermatitis atópica, la forma más común de eccema, es una enfermedad inflamatoria crónica. Es su forma moderada, se caracteriza por erupciones que pueden cubrir potencialmente gran parte del cuerpo, y puede incluir picazón intensa y persistente, lesiones cutáneas y sequedad de la piel, grietas, enrojecimiento, formación de costras y exudación.
Un mal control de la dermatitis atópica puede tener un impacto físico, emocional y psicosocial, causando trastornos del sueño, síntomas de ansiedad y depresión, y sentimientos de aislamiento. A pesar de la terapia estándar de atención, sigue existiendo una necesidad insatisfecha para muchos adolescentes con dermatitis atópica moderada a severa que a menudo tienen síntomas persistentes no controlados.
"Los adolescentes con dematitis atópica moderada a grave en la UE tienen ahora un medicamento biológico aprobado que puede controlar significativamente la persistencia, debilitando síntomas como el picazón y lesiones en la piel, así como mejorar el suelo, que es particularmente crítico en los años de formación que viven estos adolescentes", declara George D. Yancopoulos, Presidente y Director Científico en Regeneración. "Esta aprobación también proporciona a estos jóvenes pacientes una opción de tratamiento que aborda la inflamación de tipo 2 que subyace a la dermatitis atópica. Además de usos aprobados en dermatitis atópica y asma en la UE, continuamos investigando Dupixent en una amplia gama de pacientes con otras enfermedades inflamatorias de tipo 2".
Dupixent es un anticuerpo monoclonal completamente humano que inhibe la señalización de la interleucina4 (IL-4) y proteínas interleucina-13 (IL-13). Los datos de los ensayos clínicos de Dupixent han demostrado que IL-4 e IL-13 son impulsores clave en la inflamación tipo 2, que juega un papel importante en la dermatitis atópica, así como en el asma y la rinosinusitis crónica con poliposis nasal.
"Adolescentes con un control inadecuado de la dermatitis atópica moderada a grave se enfrentan a un conjunto de retos que pueden tener un impacto duradero en sus vidas. Los síntomas físicos y psicosociales pueden evitar que los adolescentes participen plenamente en actividades con sus compañeros en la escuela, deportes y pasatiempos, y a menudo pueden ser una carga seria para los miembros de la familia", señala John Reed, Jefe de Investigación y Desarrollo de Sanofi. "De nuestros ensayos de Fase3, sabemos que Dupixent redujo significativamente la picazón, ayudó a la limpiar la piel y mejoró la calidad de vida de los adolescentes en este período crítico de sus vidas".
La aprobación de la Comisión Europea se basa en datos clínicos del programa LIBERTY AD, que incluye un ensayo fundamental de Fase 3 y un ensayo se extensión abierto que evalúa la eficacia y seguridad de Dupixent en adolescentes con dermatitis atópica moderada a grave no controlada.