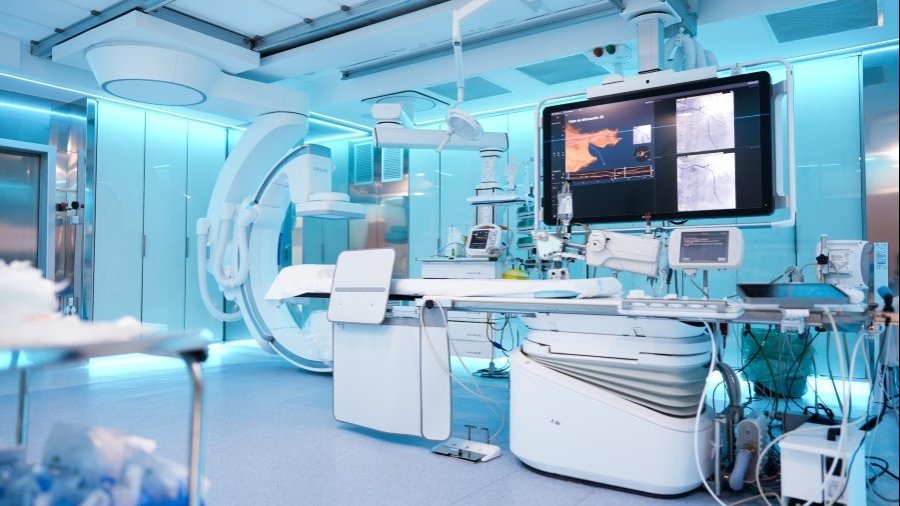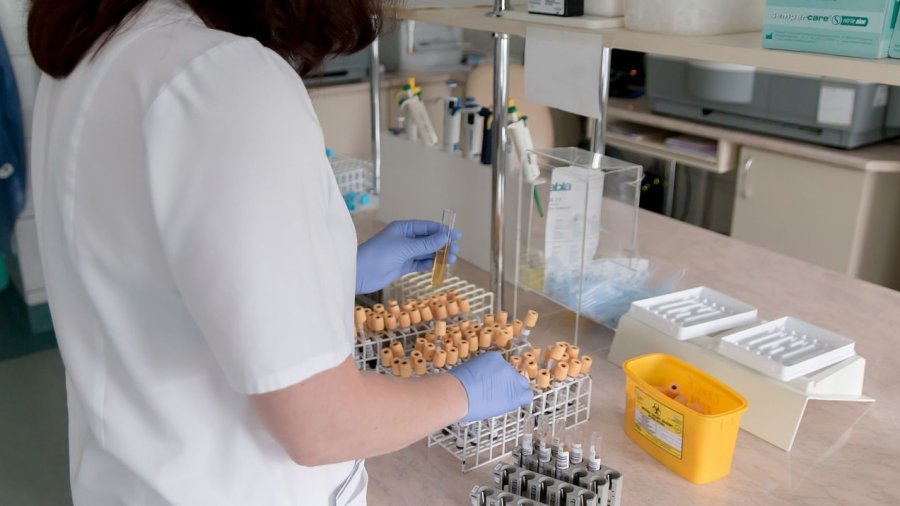
Actualmente, España es el primer país europeo y cuarto del mundo por número de ensayos clínicos contra el coronavirus.
NOTICIAS RELACIONADAS
La Unión Europea pone en marcha la Alianza de Medicamentos Críticos
La Unión Europea pone en marcha la Alianza de Medicamentos Críticos
La Aemps recibirá apoyo técnico de la CE para fortalecer su evaluación de tecnologías sanitarias
El Registro Español de Ensayos Clínicos (REEC) revela que en el primer semestre del año la Agencia Española de Medicamentos (Aemps) ha autorizado cerca de 400 ensayos clínicos para patologías distintas al coronavirus, lo que da muestras del interés por parte de los agentes implicados en la investigación clínica en España por no detener el progreso médico. A pesar de la crisis ocasionada por la pandemia, España se ha convertido en el primer país europeo y cuarto del mundo por número de ensayos clínicos contra el coronavirus, hasta sumar un centenar a día de hoy, gracias a la colaboración de la Aemps, investigadores, centros, pacientes y compañías farmacéuticas promotoras.
El compromiso y colaboración de todos los agentes públicos y privados dedicados a esta valiosa tarea han hecho posible que en ningún caso los pacientes que participan en ensayos clínicos se hayan quedado sin su tratamiento y que, sin haber acabado con el virus y siempre garantizando la seguridad de los pacientes, se haya comenzado a normalizar la situación en este terreno. A pesar de que el coronavirus ha golpeado a España más que a otros países de la Unión Europea, el proceso para retomar el ritmo habitual en la investigación clínica se está produciendo de igual manera que en otros Estados y ya se puede hablar de una recuperación casi total de la actividad, siempre en función de las características y situación de cada centro.
Lo extraordinario de esta crisis sanitaria provocó en sus inicios un colapso en los hospitales que afectó de manera directa a los ensayos clínicos en marcha, impidiendo, entre otras actividades, las visitas de seguimiento de los pacientes, la recogida de la medicación o la monitorización de los resultados in situ, lo que dejó en pausa a muchos de ellos. Sin embargo, la rápida reacción de la Aemps con medidas excepcionales para gestionar los problemas derivados de la emergencia sanitaria en materia de ensayos clínicos- y de los laboratorios promotores, en coordinación con investigadores y centros, ha permitido que en todo este tiempo los pacientes no se quedaran sin su medicamento; en algunos casos, su única esperanza para la supervivencia.
Por otra parte, sí se produjo una paralización en el reclutamiento de pacientes, motivada precisamente por las restricciones de acceso en los hospitales y la limitación de las consultas médicas a casos de urgencia. No obstante, las compañías farmacéuticas se han volcado desde el comienzo de la crisis sanitaria en tratar de que ésta afecte lo menos posible a los ensayos clínicos que se realizan en los hospitales españoles, intentando mantener la actividad sin poner en riesgo la seguridad de los pacientes. La situación está superada a día de hoy y en las últimas semanas se ha producido un fuerte impulso de los nuevos reclutamientos por parte de los investigadores principales en diferentes áreas terapéuticas.
Tras la experiencia vivida, una de las principales lecciones que ha dejado la pandemia es la importancia de la investigación biomédica como motor para la recuperación económica de nuestro país, por su incuestionable valor sanitario y también económico para pacientes, profesionales sanitarios e investigadores, centros, laboratorios promotores y autoridades sanitarias. La otra lección es el valor de la tecnología aplicada a los ensayos.
Algunas de las iniciativas que se han puesto en marcha durante la pandemia han demostrado que se puede mantener la realización de estos estudios con garantías y seguridad, pero de una manera más eficiente, por lo que desde la industria innovadora se propone combinar el modelo tradicional de desarrollo de ensayos clínicos con formatos virtuales o con la digitalización de determinados procesos, como pueden ser las reuniones telemáticas, el uso de la telemedicina o la monitorización remota con verificación de datos fuente.